某产品每件成本10元,在试销阶段每件产品的日销售价x(元)与产品的日销售量y(件)之间的关系如下表:
(2)要使每日的销售利润最大,每件产品的销售价应定为多少元?此时每日销售利润是多少元? |
(1)设经过点(15,25)(20,20)的函数关系式为y=kx+b.
∴
,15k+b=25 20k+b=20
解得:
.k=-1 b=40
∴y=-x+40.
∴y与x的函数关系式是y=-x+40;
(2)设每日的销售利润为m元.
则m=y(x-10)
=(-x+40)(x-10)
=-x2+50x-400
=-(x-25)2+225,
∴当x=25时,m最大=225.
答:每件产品的销售价定为25元时,每日销售利润最大是225元.

 CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化: 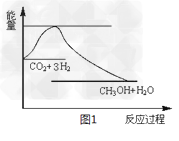
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。