根据下表信息回答:
| 族 周期 | IA | 0 | ||||||
| 1 | 1 H 1.008 | ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2 He 4.003 |
| 2 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.8l | 6 C 12.01 | 7 N 14.0l | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 3 | 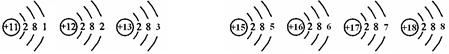 | Z | ||||||
(1)第10号元素的名称是 ,氧元素的原子失去电子形成的阴离子符号是 ,其离子结构示意图是 。
(2)第2周期共有 种固体非金属元素,该周期元素原子的核外 数相同。
(3)9号元素和17号元素的化学性质相似的原因是它们的 数相同; Z元素和8号元素形成化合物的化学式为 。
(1)氖 ,O2- 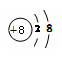 (2)2,电子层, (3) 最外层电子, SiO2
(2)2,电子层, (3) 最外层电子, SiO2
题目分析:(1)根据元素周期表的一个小格的内容分析,第10号元素是Ne,故化学名称是氖;原子核外最外层电子数少于4个,一般容易失去电子形成阳离子;原子核外最外层电子数多于4个的,一般容易得到电子形成阴离子,由于氧元素的原子的最外层电子数为6,多于4个,故容易得到2个电子而达到8个电子的相对稳定结构,形成带2个单位负电荷的阴离子,其符号为O2-,其离子结构示意图是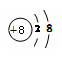 。
。
(2)根据原子最外层电子数的特点分析,非金属元素的原子最外层电子的数目一般多于4个,金属元素的原子最外层电子的数目一般少于4个,故第2周期中属于非金属元素的有 B、C、N、O、F,其中B、C属于固体非金属元素;该周期的元素原子的核外电子层数和周期数相同。
(3)元素的化学性质与原子核外的最外层电子数有密切关系,原子核外的最外层电子数相同,化学性质相似,由于9号元素和17号元素的原子核外的最外层电子数都是7,故它们的化学性质相似。由于Z元素是第14号元素,故为Si,8号元素为O,故它们形成化合物的化学式为SiO2。
点评:理解和熟练掌握元素周期表的特点及其应用,是解答本题的关键,并能根据原子结构示意图判断元素的化合价,会根据化合价书写化学式。
