问题
填空题
随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。
工业上合成甲醇一般采用下列反应,
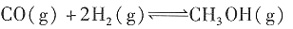 ΔH=akJ/mol
ΔH=akJ/mol
下表给出该反应在不同温度下的化学平衡常数(K):

①由表中数据判断,该反应是()反应(放热或吸热)。
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中充分反应达到平衡后,测得c(CO)=0.5mol/L,则此时的温度为()℃。
答案
参考答案:
①该反应的化学平衡常数随温度的升高而减小,因此升高温度向逆反应方向移动,而升高温度向吸热反应方向移动,故该反应是放热反应。
②CO的起始浓度为1.0mol/L,平衡浓度为0.5mol/L,所以转化浓度为0.5mol/L。

该温度下的平衡常数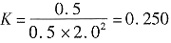 ,则此时的温度为310℃。
,则此时的温度为310℃。
