问题
单项选择题
莫尔盐[(NH4)2Fe(SO4)2·6H2O]常作氧化还原滴点法的基准物质,在0.1mol/L该盐的溶液中,下列浓度关系表达不正确的是().
A.c(H+)=c(OH-)+c(NH3·H2O)+c[Fe(OH)2]
B.c(NH3·H2O)+c(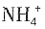 )=0.2mol/L
)=0.2mol/L
C.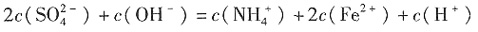
D.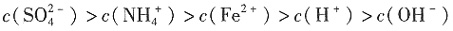
答案
参考答案:A
解析:
根据质子守恒,水电离产生的H+与OH-数目相等,结合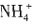 +H2O====-H++NH3·H2O和Fe2++2H2O====Fe(OH)2+2H+,可得c(H+)=c(OH-)+c(NH3·H2O)+2c[Fe(OH)2],A选项错误。根据
+H2O====-H++NH3·H2O和Fe2++2H2O====Fe(OH)2+2H+,可得c(H+)=c(OH-)+c(NH3·H2O)+2c[Fe(OH)2],A选项错误。根据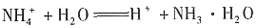 知,氮原子有两种存在形式,即
知,氮原子有两种存在形式,即 和NH3·H2O,根据氮原子守恒,c(NH3·H2O)+c(
和NH3·H2O,根据氮原子守恒,c(NH3·H2O)+c( )=0.2mol/L,B选项正确。在(NH4)2Fe(SO4)2·6H2O溶液中,存在
)=0.2mol/L,B选项正确。在(NH4)2Fe(SO4)2·6H2O溶液中,存在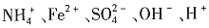 ,由电荷守恒得
,由电荷守恒得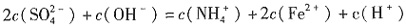 ,C选项正确。在(NH4)2Fe(SO4)2·6H2O溶液中,存在
,C选项正确。在(NH4)2Fe(SO4)2·6H2O溶液中,存在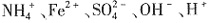 ,由于
,由于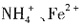 都水解,导致二者的浓度都减小,即
都水解,导致二者的浓度都减小,即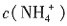 <0.2mol/L,c(Fe2+)<0.1mol/L,
<0.2mol/L,c(Fe2+)<0.1mol/L, 、Fe2+水解使溶液呈酸性,即c(H+)>c(OH-);因为盐类水解程度较小,因此c(Fe2+)>c(H+),则c(
、Fe2+水解使溶液呈酸性,即c(H+)>c(OH-);因为盐类水解程度较小,因此c(Fe2+)>c(H+),则c( )>c(
)>c(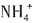 )>c(Fe2+)>c(H+)>c(OH-),D选项正确。故本题选A。
)>c(Fe2+)>c(H+)>c(OH-),D选项正确。故本题选A。
