问题
单项选择题
(一)请根据下表所提供的信息回答问题
一个国家或地区的国际竞争力排名,是通过其经济绩效、政府效率、企业效率和基础设施四个要素的排名综合而成的。根据瑞士洛桑管理学院的《全球竞争力年鉴》(2003年、2004年),选择六个国家与我国的国际竞争力进行比较,如下表:
我国与其它六国国际竞争力及其四要素排名比较
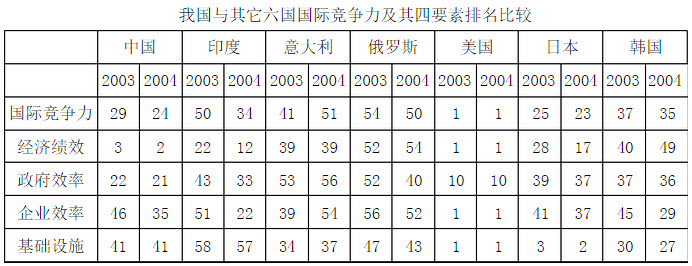
2004年,哪个国家的企业效率排名得到很大的提升,并一举超过韩国()。
A.日本
B.俄罗斯
C.印度
D.意大利
答案
参考答案:C
解析:
印度。
