工业上“固定”和利用CO2能有效地减轻“温室效应”。目前工业上利用CO2来生产燃料甲醇,可将CO2变废为宝。已知常温常压下:
①
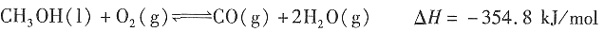
②
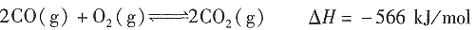
已知25℃时,乙酸和碳酸的电离平衡常数如下表:
| 物质的化学式 | CH3COOH | H2CO3 | |
| 电离平衡常数 | K=1.8×10-3 | K1=4.3×10-7 | K2=5.6×10-11 |
①用饱和氨水吸收CO2可得到NH4HCO3溶液。若已知CH3COONH4溶液pH=7,则NH4HCO3溶液显______(填“酸性”、“碱性”或“中性”)。
②在25℃时,在乙酸溶液中加入一定量的NaHCO3,所得混合液的pH=6,那么混合液中
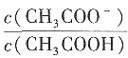 =______。
=______。
③向0.1mol·L-1CH3COOH溶液中加入少量CH3COONa晶体,有关说法正确的是______(填代号)。
a.溶液的pH增大 b.CH3COOH的电离程度增大
c.溶液的导电能力减弱 d.溶液中c(OH-)·c(H+)不变
参考答案:①碱性
②18
③a、d
解析:
(1)①

②
 ΔH=-566kJ/mol
ΔH=-566kJ/mol
-②-2×①得

则上式ΔH=566kJ/mol+354.8kJ/mol×2=+1275.6kJ/mol
(2)①

②由图像可知,H2的浓度没有变化,但是其转化率和转化速率均增大,所以改变的条件为增大二氧化碳的浓度。
(3)①由电离平衡常数可知,CH3COOH的酸性大于H2CO3,CH3COONH4溶液pH=7,则NH4HCO3溶液的pH>7,显碱性。
②


则
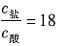
即

③略。
