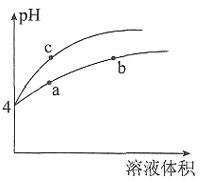
某温度下,体积和pH值都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是()。
A.a、c两点溶液的导电能力相同
B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-)
C.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc
D.a、b、c三点溶液水的电离程度a>b>c
参考答案:D
解析:
盐酸溶液中的氢离子主要是盐酸电离出来的,盐酸完全电离,体积和pH都相同的盐酸和氯化铵溶液加水稀释的过程中,盐酸不能继续电离,盐酸溶液中氢离子浓度变化大;氯化铵溶液中铵离子可继续水解,溶液中的氢离子浓度变化小,所以含c点的pH变化曲线是盐酸溶液的,含a、b点的pH变化曲线是氯化铵溶液的。
A项,溶液的导电能力和溶液中自由移动离子的多少有关,当溶液的体积相等时,a、c两点溶液的离子浓度不一样,所以导电能力不一样,故A错误;B项,b点溶液中,根据质子守恒,得出c(OH-)+c(NH3·H2O)=c(H+),故B错误;C项,用等浓度。NaOH溶液和等体积b、c处溶液反应,b点为铵根水解导致溶液呈酸性,b点溶液中铵根和氢离子均消耗NaOH,而c点只有盐酸消耗NaOH(盐酸完全电离),故消耗NaOH溶液体积Vb<Vc,故C错误;D项,盐酸电离出的氢离子抑制了水的电离,所以c点溶液中水的电离程度最小;水解促进水的电离,由于氯化铵溶液中的氢离子来自于铵根离子水解生成的氢离子,氢离子浓度越大,说明水解程度越大,水的电离程度越大,a点的pH<b点的pH,说明a点酸性大于b点酸性、a点氢离子的浓度大于b点氢离子的浓度,所以a、b两点溶液水的电离程度a>b,综上所述,a、b、c三点溶液水的电离程度a>b>c,故D正确。故选D。
