1909年,化学家哈伯用氮气和氢气在高温高压条件下首次合成了氨气,反应原理是N2+3H2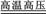 2NH3。氨气在氧气中能燃烧,燃烧时放出大量热量。近年来,科学家发现用催化剂在常温下就能合成氨气,使其有望成为替代氢能的新一代能源。
2NH3。氨气在氧气中能燃烧,燃烧时放出大量热量。近年来,科学家发现用催化剂在常温下就能合成氨气,使其有望成为替代氢能的新一代能源。
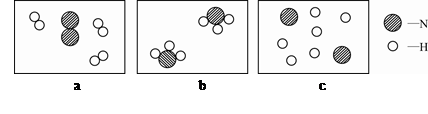
(1)若用下面三幅模型图表示合成氨气的过程,则从反应开始到完成的排列顺序为
___(用字母表示)。
(2)氮氧化物有毒性,但在一定条件下,氨气燃烧产物却没有任何污染,该反应原理是4NH3+3O2 2X+6H2O,其中X是____。
2X+6H2O,其中X是____。
(3)如果氨气不慎泄露,在关闭阀门的前提下,喷洒大量水雾即可。由此可知氨气可能具有的一条性质是______________。
(1)acb (2)N2 (3)极易溶于水(或易溶于水,能溶于水,能与水反应等合理答案即可)
题目分析:(1)化学反应的过程是分子分裂成原子,原子重新组合成新物质的分子的过程,图中a表示的,是氢分子和氮分子是反应开始前的状态,c表示是氮原子和氢原子,是反应中间状态,b表示的是氨分子,是反应后的状态;(2)从4NH3+3O2 2X+6H2O可以看出,反应物中有4个氮原子、12个氢原子和6个氧原子,而生成物中的6个水分子中含有12个氢原子和6个氧原子,根据反应前后原子的种类和数目不变可知,2X中含有4个氮原子,1个X中含有2个氮原子故X是N2;(3)根据题目提供的信息不难推断,氨气极易溶于水或易溶于水。
2X+6H2O可以看出,反应物中有4个氮原子、12个氢原子和6个氧原子,而生成物中的6个水分子中含有12个氢原子和6个氧原子,根据反应前后原子的种类和数目不变可知,2X中含有4个氮原子,1个X中含有2个氮原子故X是N2;(3)根据题目提供的信息不难推断,氨气极易溶于水或易溶于水。
