粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质.
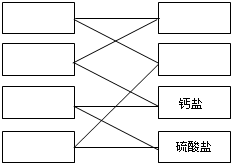
(1)化学学习中分类的方法是无可替代的.如图是对粗盐中可溶性杂质的一种分类,请将粗盐中的杂质CaCl2、MgCl2、CaSO4、MgSO4的化学式填入左列的方框中,根据分类方法将镁盐、氯化物填入方框中.
(2)从粗盐制得精盐的过程如下:
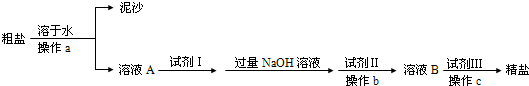
①各操作分别是:操作a______、操作c______.
②各试剂分别是:试剂Ⅰ______、试剂Ⅱ______、试剂Ⅲ______.
③加入试剂Ⅱ所发生反应的离子方程式为______、______.
④操作b与试剂Ⅲ的顺序能否交换?为什么?______.
(1)CaCl2、MgCl2、CaSO4、MgSO4中技术与硫酸盐有属于钙盐的是硫酸钙,此外硫酸镁属于硫酸盐类,也属于镁盐,氯化镁也属于镁盐,也属于氯化物,氯化钙也属于氯化物,据此可知氯化镁既是氯化物又是镁盐,故答案为:

(2)粗盐溶于水,过滤,可以将泥沙除掉,除去硫酸根离子用钡离子沉淀,可以加氯化钡,除去镁离子用氢氧根离子进行沉淀,可以加氢氧化钠,除去钙离子用碳酸根离子进行沉淀,可以加碳酸钠,过量的钡离子需要用碳酸钠除去,最后再向滤液中加入适量的盐酸得到精盐水,加入试剂的原则是:碳酸钠加在氯化钡以后,最后加入盐酸,出去氢氧化钠和过量的碳酸钠.
①粗盐溶于水,过滤,可以将泥沙除掉,最后将溶液蒸发,可以除去过量的盐酸,故答案为:过滤;蒸发;
②过程中先后加入的试剂依次是BaCl2溶液、氢氧化钠、Na2CO3溶液、盐酸,故答案为:BaCl2溶液;Na2CO3溶液;盐酸;
③加入碳酸钠可以和氯化钡反应,可以氯化钙发生反应,反应的离子方程式为:Ba2++CO32-=BaCO3↓、Ca2++CO32-=CaCO3↓,故答案为:Ba2++CO32-=BaCO3↓;Ca2++CO32-=CaCO3↓;
④试剂Ⅲ是盐酸、可以和氢氧化镁、碳酸钙以及碳酸钡发生反应生成氯化镁、氯化钙、氯化钡,这样除去的杂质离子又会生成,所以操作b与试剂Ⅲ的顺序不能交换,
故答案为:不能交换,因盐酸能将前面生成的沉淀氢氧化镁、碳酸钙和碳酸钡溶解而产生新的杂质.
