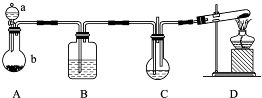
纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙.
供选择的药品:
①石灰石
②氯化铵
③氢氧化钙
④饱和氯化钙溶液
⑤浓硫酸
⑥6mol•L-1盐酸⑦饱和食盐水⑧饱和NaHCO3溶液
(1)装置A中,仪器a的名称是______,仪器b中发生反应的离子方程式为______.装置D的试管中发生反应的化学方程式为______.装置B中盛放的溶液是______(填药品序号).
(2)设计一个简单的实验方案,判断所得碳酸钙颗粒是否为纳米级.______.(简述实验的步骤、现象和结论)
(3)通入适量气体后,C装置中物质恰好完全反应,过滤,所得滤液显______(填“酸”、“碱”、“中”之一)性,原因是______(用离子方程式表示).
(4)上述装置存在一处缺陷,该缺陷为______.
(1)仪器a的名称是分液漏斗;仪器b中为碳酸钙与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑;装置D中制取氨气,化学方程式为2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;饱和NaHCO3溶液可除掉挥发出来的氯化氢,故答案为:分液漏斗;CaCO3+2H+=Ca2++H2O+CO2↑;2NH4Cl+Ca(OH)2 △ .
CaCl2+2NH3↑+2H2O; ⑧; △ .
(2)将少量碳酸钙加水充分搅拌,看是否有丁达尔效应,若有丁达尔效应,则说明为纳米级,故答案为:将少量碳酸钙加水充分搅拌,用一束可见光照射,观察是否发生丁达尔现象,若有丁达尔现象则为纳米级,若没有丁达尔现象则不是纳米级;
(3)氯化铵在水中发生水解显酸性,离子方程式:N
+H2OH +4
NH3•H2O+H+,故答案为:酸; N △ .
+H2OH +4
NH3•H2O+H+; △ .
(4)该装置尾气未处理,故答案为:无尾气吸收装置.
