在一条鱼、虾绝迹的小河边有四座工厂:甲、乙、丙、丁(如图所示),它们排出的废液里,每个工厂只含有Na2CO3、FeCl3、Ca(OH)2、HCl中的一种.某中学环保小组对河水检测时发现:①甲处河水呈乳白色,②乙处河水呈红褐色,③丙处河水由浑变清,④丁处产生气泡,河水仍清,⑤M处水样的pH小于7.请判断:
(1)四座工厂排出的废液里含有的污染物:
甲______,乙______,
丙______,丁______.
(2)写出乙、丁两处发生反应的离子方程式:乙______.丁______.
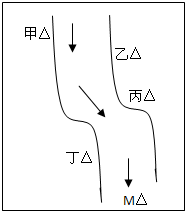
由甲处河水呈乳白色,我们可得在甲处应含有Ca(OH)2;
乙处河水呈红褐色,我们可知乙在甲处的下方且乙排放出的是FeCl3;
丙处河水由浑变清,我们可得丙处在甲乙的下方且丙处排放出的是HCl;
丁处产生气泡,河水仍清,说明丁在丙的下方且含有碳酸钠;
M在工厂的下方,所以M处的河水中肯定含有的离子有:Na+、Cl-、Ca2+,
故答案为:Ca(OH)2;FeCl3;HCl;Na2CO3;
(2)在乙处,是氯化铁和氢氧化钙之间的反应,实质是:Fe3++3OH-=Fe(OH)3,在丁处,是盐酸和碳酸钠之间的反应,实质是:CO32-+2H+═CO2↑+H2O,
故答案为:Fe3++3OH-=Fe(OH)3;CO32-+2H+═CO2↑+H2O.
