问题
填空题
(1)常温时向水中加入少量固体MgCl2,水的电离被______(填“促进”或“抑制”);与纯水相比,所得溶液中Kw______(填“变大”、“变小”或“不变”)。
(2)实验室中利用复分解反应制取Mg(OH)2。实验数据和现象如下表所示(溶液体积均取用1mL)

① 现象III是___________________;
② 分析I、II实验现象不同的原因是__________________;
③ MgCl2溶液和氨水混合后存在下列化学平衡:Mg2+(aq) + 2NH3·H2O(aq) 2NH4+(aq) + Mg(OH)2(s) 利用化学平衡常数的表达式,分析实验IV、V产生不同现象的原因:______________________。
2NH4+(aq) + Mg(OH)2(s) 利用化学平衡常数的表达式,分析实验IV、V产生不同现象的原因:______________________。
答案
(1)促进;不变
(2)①生成白色沉淀;②NH3·H2O是弱电解质,部分电离,溶液中c(OH-)很小,NaOH是强电解质,完全电离,溶液中c(OH-)很大
③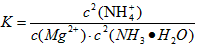 ,c(NH3·H2O)、c(Mg2+)改变相同的程度,c2(NH3·H2O)的影响更大(或起主要作用)
,c(NH3·H2O)、c(Mg2+)改变相同的程度,c2(NH3·H2O)的影响更大(或起主要作用)

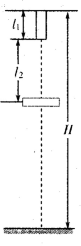
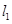 =5m的竖直杆上端距地面H=50m,杆正下方距杆下端
=5m的竖直杆上端距地面H=50m,杆正下方距杆下端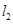 ="12" m处有一薄圆环.杆由静止释放,1s后圆环也由静止释放,杆和环均不转动,不计空气阻力,取10g=
="12" m处有一薄圆环.杆由静止释放,1s后圆环也由静止释放,杆和环均不转动,不计空气阻力,取10g=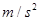 ,求:
,求: