问题
问答题
称取红丹(Pb3O4)0.1000g。用:HCL溶解,调节溶液至弱酸性,加入K2CrO4,使Pb2+沉淀为PbCrO4,将沉淀过滤、洗涤,然后将其溶解于HCL,加入过量KI,析出的I2以淀粉为指示剂,用0.1000 mol*L-1Na2S2O3标准溶液滴定,用去了12.85ml,计算试样中Pb3O4的含量。(M (Pb3O4)=685.6)
答案
参考答案:
解析:有关反应式为:
Pb3O4+8H+=3Pb2++4H2O
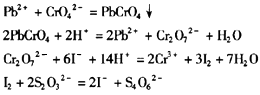
由上述反应可知
