原子序数依次增大的A、B、C、D都是元素周期表中前20号元素,B、C、D同周期,A、D同主族,且A的原子结构中最外层电子数是电子层数的3倍.D的最高价氧化物对应的水化物为强酸,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水.根据以上信息,回答下列问题:
(1)D的离子结构示意图是______,A和B形成的化合物中含有非极性共价键的是______,该物质的电子式是______.
(2)加热时,D单质能跟B的最高价氧化物对应水化物的浓溶液发生氧化还原反应,生成两种盐,该氧化还原反应的离子方程式为______.
(3)写出C的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物反应的离子方程式______.
“B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水”且B、C、D原子序数依次增大,可知C的最高价氧化物对应的水化物具有两性,即Al(OH)3,故C为Al;Al(OH)3只能和强碱反应,故B为Na;A的原子结构中最外层电子数是电子层数的3倍,A为氧;A、D同主族,D为硫.所以,A、B、C、D依次为O、Na、Al、S.
(1)D为硫,最外层6个电子,容易得2个电子达稳定结构;A、B分别是O、Na,形成的化合物中含有非极性共价键的是过氧化钠,该物质中既有离子键又有非极性共价键.
故答案为:
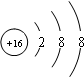
Na2O2
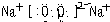
(2)D单质是S,B的最高价氧化物对应水化物是氢氧化钠,硫单质的化合价是0价,发生氧化还原反应时既做氧化剂又做还原剂,根据化合价变化规律,形成的离子分别是硫离子和亚硫酸根离子,故答案为:3S+6OH-
2S2-+SO32-+3H2O 加热 .
(3)C的最高价氧化物对应的水化物是Al(OH)3,B的最高价氧化物对应的水化物是氢氧化钠,氢氧化铝和氢氧化钠反应生成盐和水,氢氧化铝不溶于水,写化学式,故答案为:Al(OH)3+OH-=AlO2-+2H2O
