现有六种元素A、B、C、D、E均为周期表中前18号元素,且原子序数依次增大.已知A和B是形成化合物种类最多的两种元素;B元素和C元素通常形成电子数为14或22的化合物.D元素的原子半径是短周期主族元素中最大的;E元素是地壳中含量最高的金属.请回答以下问题:
(1)请画出D的离子结构示意图______;由C、A两种元素形成的18电子化合物的电子式为______;
(2)E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式:______;
(3)由以上五种元素两两组合所形成的化合物中,既含有离子键又含有非极性共价键的常见化合物有______(填化学式);它的主要用途是______,它与水反应的离子方程式______.
A和B是形成化合物种类最多的两种元素,应为H和C两种元素,所形成的化合物多为有机物,种类繁多,B元素和C元素通常形成电子数为14或22的化合物,这两种化合物分别
为CO、CO2,则可推知A为H元素,B为C元素,C为O元素,D元素的原子半径是短周期主族元素中最大的,应为Na元素,E元素是地壳中含量最高的金属,为Al元素,
(1)D元素的原子半径是短周期主族元素中最大的,应为Na元素,Na+离子有11个质子,核外有10个电子,其离子结构示意图为
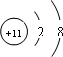
,由C、A两种元素形成的18电子化合物为H2O2,为共价化合物,氧原子之间有一个共用电子对,满足8电子稳定结构,电子式为
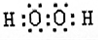
,故答案为:
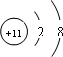
;
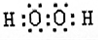
;
(2)该反应为Al2O3和NaOH之间的反应,Al2O3具有两性,与NaOH反应生成盐和水,反应的离子方程式为Al2O3+2OH-=2AlO-2+H2O,
故答案为:Al2O3+2OH-=2AlO-2+H2O;
(3)Na2O2既含有离子键又含有非极性共价键,具有强氧化性,与水反应生成氧气,常用于供氧剂和漂白剂,与水反应的离子方程式为 2Na2O2+2H2O=4Na++4OH-+O2↑,
故答案为:Na2O2;供氧剂、漂白剂;2Na2O2+2H2O=4Na++4OH-+O2↑.
