问题
选择题
下列离子方程式错误的是( )
A.工业上用氯气通入石灰乳制漂白粉:2Ca(OH)2+Cl2=Ca(ClO)2+Ca2++Cl-+2H2O
B.向污水中投放明矾,生成能凝聚悬浮物的粒子:Al3++3H2O
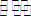
Al(OH)3+3H+
C.用Na2S除去废水中的Hg2+:Hg2++S2-=HgS↓
D.用氨水吸收硫酸工业尾气中的SO2:SO2+2NH3+H2O=2NH+4+SO2-3
答案
A、氯气通入石灰乳制漂白粉的离子方程式为:2Ca(OH)2+Cl2=2ClO-+2Ca2++Cl-+2H2O,次氯酸钙是可溶于水的盐,氢氧化钙在离子方程式中遵循“清离浊分”的处理原则,故A错误;
B、明矾中的铝离子水解生成的氢氧化铝具有净水作用,原理是:Al3++3H2O
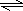
Al(OH)3+3H+,故B正确;
C、Na2S中的钠离子和废水中的Hg2+反应生成的硫化汞是难溶于水的沉淀,即Hg2++S2-=HgS↓,故C正确;
D、氨水显碱性,能和酸性气体二氧化硫反应生成盐,即SO2+2NH3+H2O=2NH4++SO32-,故D正确.
故选A.
