问题
问答题
已知反应:3NO2+H2O═2HNO3+NO,回答下列问题:
(1)该反应的离子方程式为______.
(2)氧化剂与还原剂的质量比为______,氧化产物与还原产物的物质的量之比为______.
(3)在标准状况下,3.36L NO2与H2O完全反应转移的电子数目为______.
(4)用单线桥标出该反应中电子转移的方向和数目______.
(5)写出HNO3与石灰水反应的离子方程式______.
答案
(1)反应3NO2+H2O═2HNO3+NO的离子方程式为3NO2+H2O═2H++2NO3-+NO,故答案为:3NO2+H2O═2H++2NO3-+NO;
(2)反应二氧化氮中氮元素化合价既升高也降低,二氧化氮既作氧化剂又作还原剂,3mol的NO2中,2mol做还原剂,1mol做氧化剂,氧化剂与还原剂的质量比为1:2,
氧化产物是2NO3-,还原产物是NO,所以氧化产物与还原产物的物质的量之比为2:1,故答案为:1:2;2:1;
(3)反应3NO2+H2O═2HNO3+NO转移的电子为2mol,即3mol的NO2反应,转移2mol电子,当在标准状况下,3.36L(即0.15mol) NO2与H2O完全反应转移的电子为0.1mol,
数目为0.1NA,故答案为:0.1NA;
(4)该反应中,只有氮原子化合价变化,电子转移的方向和数目为
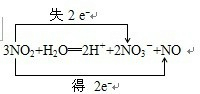
,故答案为:

;
(5)HNO3(是强酸)与石灰水(是强碱)反应生成硝酸钙(可溶于水的盐)和水,离子方程式为H++OH-=H2O,故答案为:H++OH-=H2O.
