A、B、C、D、E是五种原子序数依次增大的短周期元素,B是地壳中含量最多的元素.已知A、C及B、E分别是同主族元素,且B、E两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍.处于同周期的C、D、E元素中,D是该周期金属元素中金属性最弱的元素.
(1)A、B、C形成的化合物的电子式为______;
(2)一点温度下,浓度相同的B、C、D组成的化合物的水溶液与A、C、E组成的化合物的水溶液的pH______>______(填化学式)
(3)D与C元素最高价氧化物对应水化物反应的离子方程式______
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式______
(5)A单质和B单质能构成电池,该电池用多孔惰性电极浸入浓KOH溶液,两极分别通入A单质和B单质,电池的负极通入的是______气体,电极反应式______;
(6)通常条件下,C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6kJ,试写出表示该热量变化的离子方程式______.
(1)A为H,B为O,C为Na,D为Al,E为S,A、B、C形成的化合物为氢氧化钠,电子式为
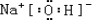
,故答案为:
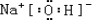
;
(2)B、C、D组成的化合物为NaAlO2,A、C、E组成的化合物为NaHS,氢氧化铝为两性氢氧化物,硫化氢为弱酸,故酸性硫化氢大于氢氧化铝,故浓度相同两种混合物水解时,碱性NaAlO2>NaHS,故答案为:NaAlO2>NaHS;
(3)C元素最高价氧化物对应水化物为氢氧化钠,D为Al,故反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体,可以为硫酸氢钠与亚硫酸氢钠的反应,离子方程式如下H++HSO3-=SO2↑+H2O,
故答案为:H++HSO3-=SO2↑+H2O;
(5)氢气和氧气组成的燃料电池,负极为氢气,电极反应为H2+2OH--2e-=2H2O,故答案为:氢气;H2+2OH--2e-=2H2O;
(6)C的最高价氧化物对应水化物为氢氧化钠2mol与E最高价氧化物对应水化物硫酸1mol的稀溶液,反应的实质为氢离子和氢氧根离子反应,故热化学方程式为H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,故答案为:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol.
