根据《公路安全保护条例》的规定,下列说法不正确的是()
A、县级人民政府交通运输主管部门或者乡级人民政府可以根据保护乡道、村道的需要,在乡道、村道的出入口设置必要的限高、限宽设施
B、车辆载运不可解体物品,车货总体的外廓尺寸或者总质量超过公路、公路桥梁、公路隧道的限载、限高、限宽、限长标准,确需在公路、公路桥梁、公路隧道行驶的,从事运输的单位和个人应当向公路管理机构申请公路超限运输许可
C、新建村镇、开发区、学校和货物集散地、大型商业网点、农贸市场等公共场所,与公路建筑控制区边界外缘的距离国道、省道不少于20米
参考答案:C

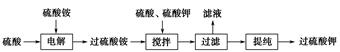
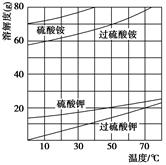
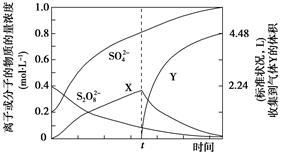
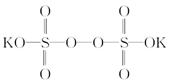 )具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下:
)具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下: