问题
单项选择题
某工厂甲车间每天产生含盐酸(HCl)0.73%的酸性废水50m3,乙车间产生含1.6%氢氧化钠(NaOH)的碱性废水,其水量和水质变化较大,采用间歇式中和池将酸碱废水进行中和处理。若处理后废水酸碱达到完全中和,则乙车间每天排出的碱性废水量应为()。(相对分子质量:HCl 36.5;Na0H 40)
A.40m3
B.30m3
C.25m3
D.20m3
答案
参考答案:C
解析:
此题的化学反应方程式为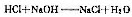
根据反应方程式计算所需NaOH的用量:盐酸(HCl)的摩尔浓度=(1000×0.73%)/36.5=0.2mol/L;
氢氧化钠(NaOH)的摩尔浓度=(1000×1.6%)/40=0.4mol/L。
当处理后废水酸碱度达到完全中和时:0.2×50=0.4X,故碱性废水的量为25m3。
见《考试教材》第2册第515页。