问题
单项选择题
某温度下, 的平衡常数
的平衡常数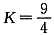 。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)(mol/L) | 0.010 | 0.020 | 0.020 |
| c(CO2)(mol/L) | 0.010 | 0.010 | 0.020 |
下列判断不正确的是()
A.平衡量,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
答案
参考答案:C
解析:
本题涉及化学平衡常数及转化率的计算。设平衡时甲中CO2的转化浓度为xmol/L,则平衡时H2、CO2、H2O、CO的浓度分别为(0.01-x)mol/L、(0.01-x)mol/L、xmol/L,根据平衡常数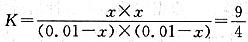 ,解得x=0.006,则甲中CO2的转化率为
,解得x=0.006,则甲中CO2的转化率为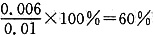 ,由于乙相对于甲增大了c(H2),因此CO2的转化率增大,A正确;设平衡时丙中CO2的转化浓度为ymol/L,则平衡时H2、CO2、H2O、CO的浓度分别为(0.02-y)mol/L、(0.02-y)mol/L、ymol/L、ymol/L,根据平衡常数
,由于乙相对于甲增大了c(H2),因此CO2的转化率增大,A正确;设平衡时丙中CO2的转化浓度为ymol/L,则平衡时H2、CO2、H2O、CO的浓度分别为(0.02-y)mol/L、(0.02-y)mol/L、ymol/L、ymol/L,根据平衡常数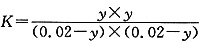
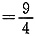 ,解得y=0.012,则丙中CO2的转化率为
,解得y=0.012,则丙中CO2的转化率为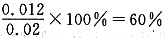 ,B正确;平衡时甲中c(CO2)=0.01-0.006=0.004(mol/L),丙中c(CO2)=0.02-0.012=0.008(mol/L),C错;反应开始时,丙中反应物浓度最大,反应速率最快,甲中反应物浓度最小,反应速率最慢,D正确。
,B正确;平衡时甲中c(CO2)=0.01-0.006=0.004(mol/L),丙中c(CO2)=0.02-0.012=0.008(mol/L),C错;反应开始时,丙中反应物浓度最大,反应速率最快,甲中反应物浓度最小,反应速率最慢,D正确。
