能正确表示下列反应的离子方程式的是
A.向次氯酸钙溶液中通入过量的CO2:Ca2++H2O+2ClO-+CO2= CaCO3↓+2HClO
B.向次氯酸钙溶液中通入SO2: Ca2++H2O+2ClO-+SO2= CaSO3↓+2HClO
C.氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+HCO- 3= CaCO3↓+H2O
D.氯化亚铁溶液中加入稀硝酸: 3Fe2++4H++NO- 3=3Fe3++2H2O+NO↑
答案:D
分析:A、向次氯酸钙溶液中通入过量CO2气体生成碳酸氢钙;
B、向次氯酸钙溶液中通入SO2气体,二氧化硫被次氯酸钙氧化为硫酸盐;
C、氢氧化钙溶液与碳酸氢镁溶液反应生成更难溶的氢氧化镁;
D、在氯化亚铁溶液中加入稀硝酸,亚铁离子被氧化为三价铁,硝酸被还原为一氧化氮;
解答:解:A、通入过量二氧化碳生成HCO3-,正确的离子方程式为ClO-+H2O+CO2═HCO3-+HClO,故A错误;
B、向次氯酸钙溶液中通入SO2气体生成硫酸钙,正确的离子方程式为SO2+ClO-+H2O=SO42-+Cl-+2H+如果溶液不是很稀,需要用CaSO4沉淀代替SO42-,同时前面加Ca2+,故B错误;
C、氢氧化钙溶液与碳酸氢镁溶液反应生成氢氧化镁沉淀,正确的离子方程式为:2Ca2++4OH-+Mg2++2HCO3-=Mg(OH)2↓+2CaCO3↓+2H2O,故C错误;
D、在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO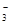 ═3Fe3++2H2O+NO↑,故D正确;
═3Fe3++2H2O+NO↑,故D正确;
故选D.
点评:本题考查离子方程式的书写,注意从电荷守恒、量不同产物不同、还原性物质遇氧化性物质发生的反应等角度判断反应是否符合实际.
