问题
单项选择题
已知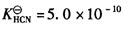 ,则0.1mol·L-1的NaCN溶液中水解常数为()。
,则0.1mol·L-1的NaCN溶液中水解常数为()。
A. 2×10-5
B.5×10-10
C. 2.2×10-6
D. 5×10-24
答案
参考答案:A
解析:
水解常数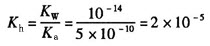
对于一元弱酸强碱的盐,如NaAc,
这类盐实际是阴离子(如Ac-)发生水解,使溶液呈碱性(pH>7)。显然,酸越弱(Ka越小),则Kh越大,即水解的程度越大,溶液的碱性越强。
对于一元弱碱强酸盐,加NH4Cl,可如上分析得出离子方程式为
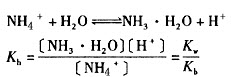
这类盐水解后,溶液呈酸性(PH<7)。且Kb越小,Kh越大,酸性越强。
弱酸弱碱盐(如NH4Ac),解离出来的阴、阳离子均能发生水解。例如弱酸弱碱盐AB水解

弱酸弱碱盐溶液的酸碱性视水解产物的Ka(HB)和Kb(AOH)的相对大小而定。
多元弱酸强碱盐的水解是分级进行的,溶液的酸性主要依据一级水解的程度来判断。
