问题
填空题
(6分)已知0.1 mol/L的NaHSO4溶液中H+的物质的量浓度为0.1mo1/L,请回答下列问题:
(1)写出NaHSO4在水溶液中电离的方程式 。
(2)若将NaHSO4与Ba (OH)2在溶液中按物质的量之比为2:1混合,化学反应的离子方程式是 。
答案
(6分)(1)NaHSO4=Na++H++SO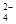 (2)2H++ SO
(2)2H++ SO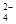 +Ba2++2OH—=2H2O+BaSO4↓
+Ba2++2OH—=2H2O+BaSO4↓
(1)硫酸氢钠在水溶液中完全电离出三种离子,即NaHSO4=Na++H++SO42-;
(2)NaHSO4与Ba (OH)2在溶液中按物质的量之比为2:1混合时,酸碱恰好中和,实质 是:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O。
