问题
选择题
25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10-5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)=Ka(HY)•c(HY) c(Y-)+c(Z-)+c(OH-) 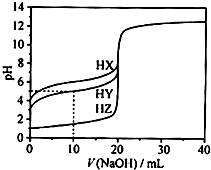
答案
A、氢氧化钠体积为0时,0.1000mol•L-1的三种酸HX、HY、HZ的PH分别为4、2.5、1,故酸性大小为HX<HY<HZ,故导电性HZ>HY>HX,故A错误;
B、当NaOH溶液滴到10ml时,溶液中c(HY)≈c(Y-),即Ka(HY)≈c(H+)=10-PH=10-5,故B正确;
C、HX恰好完全反应时,HY早已经完全反应,所得溶液为NaX和NaY混合液,酸性 HX<HX,NaY水解程度小于HX,故溶液中c(X-)<c(Y-),故C错误;
D、HY与HZ混合,溶液中电荷守恒为c(H+)=c(Y-)+c(Z-)+c(OH-);再根据HY的电离平衡常数,c(Y-)≠
,故D错误;Ka(HY)•c(HY) c(Y-)
故选B.
