已知多元弱酸在水溶液中的电离是分步进行的,且第一步的电离程度大于第二步的电离程度,第二步的电离程度远大于第三步的电离程度……今有HA、H2B、H3C三种弱酸,根据“较强酸+较弱酸盐 较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
较强酸盐+较弱酸”的反应规律,它们之间能发生下列反应:
A.HA+HC2-(少量) A-+H2C-
A-+H2C-
B.H2B(少量)+2A- B2-+2HA
B2-+2HA
C.H2B(少量)+H2C- HB-+H3C
HB-+H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中,酸性最强的是_____________。
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是_________,最难结合质子的是____________。
(3)下列反应的离子方程式正确的是____________。
A.H3C+3A- 3HA+C3-
3HA+C3-
B.HB-+A- HA+B2-
HA+B2-
(4)完成下列反应的离子方程式:
A.H3C+OH-(过量)____________________________________________________;
B.HA(过量)+C3-______________________________________________________。
(1)H2B (2)C3- HB- (3)B
(4)H3C+3OH-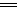 C3-+3H2O 2HA(过量)+C3-
C3-+3H2O 2HA(过量)+C3-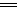 2A-+H2C-
2A-+H2C-
本题主要考查“较强酸+较弱酸盐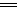 较强酸盐+较弱酸”的反应规律,由所给方程式可看出H2B酸性最强,相应的它的离子HB-最难结合质子,同样可得其他结果。
较强酸盐+较弱酸”的反应规律,由所给方程式可看出H2B酸性最强,相应的它的离子HB-最难结合质子,同样可得其他结果。
