下列化学过程及其表述正确的是 ( )
A.向NaHSO4溶液中滴入Ba(OH)2溶液至中性H++SO42-+Ba2++OH-=BaSO4↓+H2O
B.由水电离的c(H+)为10-3 mol·L-1的溶液中,Na+、NO3-、SO32-、Cl-一定能大量共存
C.向含有1molKAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量为2mol
D.可以用浓盐酸酸化的KMnO4溶液与H2O2混合,以证明H2O2具有还原性2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O
答案:C
题目分析:
本题考查的是有隐含条件的离子共存及与量有关的离子方程式书写。A.要使得溶液显中性,那么
H+与OH-的量必须1:1。1molNaHSO4电离出1molH+,1molBa(OH)2电离出2molOH-,所以n(NaHSO4):n[Ba(OH)2]=2:1。所以离子方程式应为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O。B.由水电离的c(H+)为10-3 mol·L-1,说明该溶液是促进了水的电离。水中c(H+)=10-7mol·L-1,所以该溶液中必含有弱碱阳离子(Fe3+、Cu2+ 、Al3+等)或弱酸根离子(CO32-,CH3COO-等),如果溶液中存在Fe3+,Cu2+的话,那么显然与SO32-不能大量共存。D.KMnO4溶液不能用浓盐酸酸化,酸性条件下KMnO4溶液会与浓盐酸发生反应,也不能用浓HNO3酸化(因浓HNO3本身具有强氧化性)。C.Al3++2SO42-+ 2Ba2++4OH-= 2BaSO4↓+AlO2-+2H2O,沉淀总物质的量为2mol,质量为466g。Al3++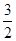 SO42-+
SO42-+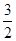 Ba2++3OH-=
Ba2++3OH-=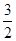 BaSO4↓+Al(OH)3↓,这种情况下,沉淀总物质的量为2.5mol,总质量为427.5g。所以C正确。
BaSO4↓+Al(OH)3↓,这种情况下,沉淀总物质的量为2.5mol,总质量为427.5g。所以C正确。
