问题
选择题
用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
A.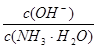
B.
C.c(H+)和c(OH-)的乘积
D.OH-的物质的量
答案
答案:B
题目分析:在氨水中存在如下电离平衡:NH3.H2O=NH4++OH-,离子方程式的电离平衡产生为
K= ×c(NH4+),用水稀释0.1mol/L氨水时,c(NH4+)变小,根据温度不变,K不变可以知道,
×c(NH4+),用水稀释0.1mol/L氨水时,c(NH4+)变小,根据温度不变,K不变可以知道, 增加,故A错误,而
增加,故A错误,而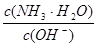 减小,所以B为本题的答案;由于温度不变,所以c(H+)和c(OH-)的乘积不变,故C错误;OH-的物质的量应该是增加,故D错误,所以本题的答案选择B。
减小,所以B为本题的答案;由于温度不变,所以c(H+)和c(OH-)的乘积不变,故C错误;OH-的物质的量应该是增加,故D错误,所以本题的答案选择B。
点评:本题考查了电离常数,水的离子积,该考点是高考考查的重点,解题的关键是温度不变,水的离子积不变,电离常数也不变,本题难度中等。
