溴及其化合物广泛应用在有机合成、化学分析等领域。
(1)海水提溴过程中溴元素的变化如下:
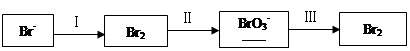
①过程Ⅰ,海水显碱性,调其pH<3.5后,再通入氯气。
ⅰ.通入氯气后,反应的离子方程式是______。
ⅱ.调海水pH可提高Cl2的利用率,用平衡原理解释其原因是______。
②过程Ⅱ,用热空气将溴赶出,再用浓碳酸钠溶液吸收。完成并配平下列方程式。
Br2+ Na2CO3=
Na2CO3= NaBrO3+
NaBrO3+ CO2+
CO2+ ______
______
③过程Ⅲ,用硫酸酸化可得Br2和Na2SO4的混合溶液。
相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是______。
(2)NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入2.6 mol NaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
| 粒子 | I2 | Br2 | IO3- |
| 物质的量/mol | 0.5 | 1.3 |
(1)①ⅰ.Cl2+2Br-=Br2+2Cl-
ⅱ.Cl2+H2O H++Cl-+HClO, 增大c(H+),平衡逆向移动,抑制Cl2与水反应
H++Cl-+HClO, 增大c(H+),平衡逆向移动,抑制Cl2与水反应
②3 3 1 3 5 NaBr
③盐酸有还原性,与溴酸根反应
(2)3
题目分析:(1)①ⅰ.通入氯气后,Cl2与Br‾反应:Cl2+2Br-=Br2+2Cl-
ⅱ.Cl2与水的反应为可逆反应:Cl2+H2O H++Cl-+HClO,降低溶液的pH,增大c(H+),平衡逆向移动,抑制Cl2与水反应。
H++Cl-+HClO,降低溶液的pH,增大c(H+),平衡逆向移动,抑制Cl2与水反应。
②根据化合价的变化和元素守恒可推知生成物为NaBr,有化合价升降法可配平化学方程式。
③HCl中Cl元素为-1价,为最低价态,所以盐酸具有还原性,能被溴酸根氧化,所溴的质量减少。
(2)根据氧化还原反应中得失电子数相等,可得5×2.6mol=2×0.5mol+6×n(IO3‾),则n(IO3‾)=2mol,根据元素守恒,原溶液中n(NaI)=0.5mol×2+2mol=3mol。
