对下列反应①KHCO3溶液与石灰水反应、②Na2SO3溶液与稀盐酸反应、③Si与烧碱溶液反应、④Fe与稀硝酸反应,改变反应物用量,不能用同一个离子方程式表示的是
A.①②③
B.①②④
C.①③④
D.②③④
答案:B
题目分析:①KHCO3溶液与石灰水反应的离子反应分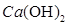 过量和不过量两种情况,对于酸式盐和碱的反应采用定“1”法,量少的设为1mol,分析如下:化学方程式和离子方程式分别为:2KHCO3+
过量和不过量两种情况,对于酸式盐和碱的反应采用定“1”法,量少的设为1mol,分析如下:化学方程式和离子方程式分别为:2KHCO3+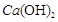 (少量)=CaCO3↓+2H2O+K2CO3,则离子方程式为:2
(少量)=CaCO3↓+2H2O+K2CO3,则离子方程式为:2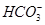 +Ca2++2
+Ca2++2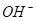 =CaCO3↓+2H2O+
=CaCO3↓+2H2O+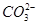 ;KHCO3+
;KHCO3+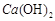 (过量)=CaCO3↓+H2O+KOH,则离子方程式为:
(过量)=CaCO3↓+H2O+KOH,则离子方程式为: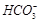 +Ca2++2
+Ca2++2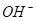 =CaCO3↓+H2O+
=CaCO3↓+H2O+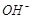 ,有分析可知①不能用一个离子方程式表示;② Na2SO3+HCl(少量)=NaHSO3+NaCl,则离子方程式为:
,有分析可知①不能用一个离子方程式表示;② Na2SO3+HCl(少量)=NaHSO3+NaCl,则离子方程式为: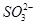 +H+=
+H+=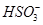 ,Na2SO3+2HCl(过量)= 2NaCl+SO2+H2O,则离子方程式为:
,Na2SO3+2HCl(过量)= 2NaCl+SO2+H2O,则离子方程式为: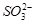 +H+= SO2↑+H2O,,由此可知②也不能用一个离子方程式表示;③Si与烧碱溶液反应只有一个离子方式,即:Si+2
+H+= SO2↑+H2O,,由此可知②也不能用一个离子方程式表示;③Si与烧碱溶液反应只有一个离子方式,即:Si+2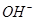 +H2O=
+H2O= +2H2↑;④Fe+4HNO3(过量)=
+2H2↑;④Fe+4HNO3(过量)=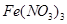 +NO↑+2H2O,则离子方程式为:Fe+4H++
+NO↑+2H2O,则离子方程式为:Fe+4H++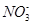 =Fe3++NO↑+2H2O,3Fe+8HNO3(少量)=3
=Fe3++NO↑+2H2O,3Fe+8HNO3(少量)=3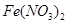 +2NO↑+4H2O,则离子方程式为:3Fe+8H++2
+2NO↑+4H2O,则离子方程式为:3Fe+8H++2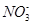 = 3Fe2++2NO↑+4H2O,由此可知④的离子方程式也不为同一离子方程式。故本题的答案为C。
= 3Fe2++2NO↑+4H2O,由此可知④的离子方程式也不为同一离子方程式。故本题的答案为C。
