在一容积固定的反应容器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下: A、 B和C均为4.0mol, D为 6.5mol, F为2.0mol,设E为xmol,x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中间位置。
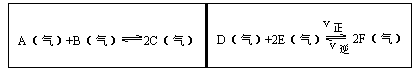
①若x=4.5,则右侧反应在起始时向______方向进行,欲使起始反应维持向该方向进行,则x的取值范围为____ 。
②若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量是否相等?______,其理由是______。
①当x=4.5时,正反应方向,x取值范围为3.5<x<7.0。②不同,理由见解析
左侧可逆反应是反应前后气体的物质的量不变的反应,右侧可逆反应的正反应是气体的物质的量缩小的反应。隔板在中间意味着左右两侧可逆反应在一定条件下达到平衡时,气体的物质的量相等。左侧气体的起始量已知,共12mol,
①当x=4.5时,气体总物质的量为13.0mol,欲使右侧反应的总物质的量为12mol,应在起始时向气体体积缩小的方向进行。欲使反应向正反应方向进行,可以通过极端假设的方法来讨论:假设平衡不移动,x="12.0" mol-6.5 mol-2.0 mol=3.5mol;假设平衡向正反应方向移动使E为0 mol,(6.5-0.5x)+(2.0+x)="12.0" mol,x="7.0" mol,故x取值范围为3.5<x<7.0。②当x的取值不同时,反应分别达到平衡的气体总物质的量均为12mol,两个反应的温度肯定不同,所以左侧中的气体A的物质的量也肯定不同。
