(9分)某学生用0.1×10×25mm3,质量分数≥99.5%的铝片和盐酸反应制取H2,实验现象见下表:

(1)写出铝片与盐酸、硫酸反应的离子方程式
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,15~20min内,反应速率逐渐减小。其原因是
(3)①根据铝片与盐酸和硫酸反应现象的差异,有学生对此现象提出如下猜想(至少要写出两种假设):
假设一:Cl-对该反应有促进作用,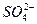 对该反应不影响。
对该反应不影响。
假设二: 。
假设三: 。]
假设四: 。
③ 请你以“假设一”为实验课题,设计实验方案探究,要求写 出主要实验步骤。
出主要实验步骤。

②将NaCl颗粒加入Al片与稀盐酸反应液中,看反应速率有无变化及变化情况,来判断Cl-是否对反应起作用。若速率加快,说明Cl-对该反应有促进作用;若速率不变,说明Cl-对该反应的速率不影响。将K2SO4颗粒加入Al片与稀H2SO4反应液中,看反应速率有无变化及变化情况,来判断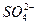 是否对反应起作用。若速率减小,说明
是否对反应起作用。若速率减小,说明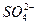 对该反应有抑制作用;若速率不变,说明
对该反应有抑制作用;若速率不变,说明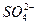 对该反应的速率不影响。(3分)
对该反应的速率不影响。(3分)
本题属于开放性试题,要求学生结合具体的实验情境,作出推断和假设,设问角度新颖,考查学生了解科学研究的基本思路和方法。(3)中答案也可能多种多样。如“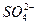 对金属铝与H+反应有抑制作用”或“
对金属铝与H+反应有抑制作用”或“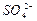 对金属铝与H+反应没有影响”或“带低电荷的阴离子对金属铝与H+反应有促进作用”等等。
对金属铝与H+反应没有影响”或“带低电荷的阴离子对金属铝与H+反应有促进作用”等等。