(11分)Ⅰ.下列各项分别与哪个影响化学反应速率因素的关系最为密切?
⑴夏天的食品易变霉,在冬天不易发生该现象_________
⑵同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢
⑶MnO2加入双氧水中放出气泡更快______________。
Ⅱ.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示:
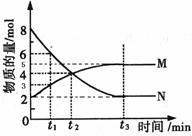
⑴比较t2时刻,正逆反应速率大小V正____ V逆。(填“>”、“=”、“<”)
⑵若t2 =2min,计算反应开始至t2时刻,M的平均化学反应速率为:________
⑶t3时刻化学反应达到平衡时反应物的转化率为_________
⑷如果升高温度则V逆____(填增大、减小或不变)
Ⅰ.⑴温度(1分)⑵反应物本身性质(1分)⑶催化剂(1分)
Ⅱ.⑴ V正> V逆(2分)⑵0.25 mol·L-1·min-1(2分)⑶75%(2分)⑷ V逆 增大(2分)
Ⅰ.考查外界条件对反应速率的影响。
(1)夏天温度高,反应速率快,所以应该是温度。
(2)镁的活泼性强于锌的,反应速率快,所以应该是反应物本身性质。
(3)双氧水的分解反应中,二氧化锰其催化剂的作用。
Ⅱ.(1)根据图像可知,t2时刻反应物的浓度减小,生成物的浓度增加,所以反应向正反应方向移动,即正反应速率大于逆反应速率。
(2)在t2时刻M的物质的量是4mol,所以M的变化量是4mol-2mol=2mol,因此其反应速率是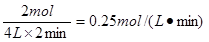 。
。
(3)t3时刻反应物N的物质的量是2mol,变化量是8mol-2mol=6mol,所以反应物的转化率为6÷8×100%=75%。
(4)升高温度反应速率都是增大的。
