问题
填空题
利用催化剂可使NO和CO发生反应:2NO(g)+2CO(g)2CO2(g)+N2(g) ΔH<0。

已知增大催化剂的比表面积可提高化学反应速率。为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验 编号 | T(℃) | NO初始浓度 (mol·L-1) | CO初始浓度 (mol·L-1) | 催化剂的比表 面积(m2·g-1) |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 1.2×10-3 | 124 | ||
| Ⅲ | 350 | 82 |
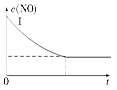
(2)实验Ⅰ中,NO的物质的量浓度(c)随时间(t)的变化如图所示。请在给出的坐标图中画出实验Ⅱ、Ⅲ中NO的物质的量浓度(c)随时间(t)变化的曲线,并标明各曲线的实验编号。
答案
(1)
| 实验 编号 | T(℃) | NO初始浓度 (mol·L-1) | CO初始浓度 (mol·L-1) | 催化剂的比表 面积(m2·g-1) |
| Ⅰ | ||||
| Ⅱ | 280 | 5.8×10-3 | ||
| Ⅲ | 1.2×10-3 | 5.8×10-3 |
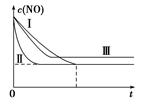
(2)
(1)在其他量相同的情况下,才能判断变量对速率的影响,要验证温度对速率的影响,催化剂的比表面积、反应物的初始浓度等要相同;同理,验证催化剂的比表面积对速率的影响,温度、反应物的初始浓度要相同。
(2)Ⅰ、Ⅱ的区别是催化剂的比表面积不同,因此Ⅱ的反应速率较快,但催化剂不影响平衡的移动。Ⅰ、Ⅲ的区别是温度变化,温度升高,化学反应速率加快,达到平衡的时间缩短,NO转化率降低,故最终Ⅲ中c(NO)较Ⅰ、Ⅱ中c(NO)大。
