向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图一所示.图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件.已知t3~t4阶段使用了催化剂;图一中t0~t1阶段c(B)未画出.

(1)若t1=15min,则t0~t1阶段以C浓度变化表示的反应速率为v(C)=______.
(2)t4~t5阶段改变的条件为______,B的起始物质的量为______.
(3)判断图一中可逆反应达到平衡状态的依据是(填序号)______.
①2v正(A)=3v逆(C)
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④A、B、C的浓度都不再发生变化
(4)t5~t6阶段保持容器内温度不变,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,写出此温度下该反应的热化学方程式:______.
(5)在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为______.
(1)v=
=△c △t
=0.02 mol/(L?min),故答案为:0.02 mol/(L?min);0.6mol/L-0.3mol/L 15min
(2)结合图一可知,A的变化为0.2mol/L,C的变化量为0.3mol/L,化学反应的速率之比等于化学方程式前的计量系数比,
可写出该反应的方程式为2A(g)+B(g)

3C(g),压强减小,正逆反应速率减小,应反应前后气体的化学计量数之和相等,则改变压强平衡不移动,所以t4~t5阶段改变的条件为减小压强,
B的平衡浓度是0.4mol/L,根据方程式可知,浓度的改变值与化学计量数呈正比,C改变0.3mol/L,则B改变0.1mol/L,
所以起始时应为0.5mol/L,起始2molA所对应的浓度为1mol/L,则体积应是2L,
所以B的起始物质的量为0.5mol/L×2L=1mol,
故答案为:减小压强; 1.0 mol;
(3)①反应达平衡状态时,正逆反应速率相等,则有3v正(A)=2v逆(C),故①错误;
②因气体的质量不变,容器的体积不变,则反应无论是否达到平衡状态,密度都不变,不能作为判断是否达到平衡的依据,故②错误;
③反应前后气体的物质的量不变,质量不变,混合气体的平均相对分子质量不变,不能作为判断是否达到平衡的依据,故③错误;
④当达到平衡状态时,A、B、C的浓度都不再发生变化,可作为平衡状态的判断依据,故④正确,
故答案为:④;
(4)根据方程式计算,若A的物质的量共变化了0.01mol,而此过程中容器与外界的热交换总量为a kJ,则反应2molA时,交换热量200akJ,而由图象可知,t5~t6阶段应为升高温度,正反应速率大于逆反应速率,平衡向正反应方向移动,则正反应为吸热反应,所以热化学方程式为2A(g)+B(g)

3C(g)△H=+200a kJ/mol,
故答案为:2A(g)+B(g)

3C(g)△H=+200a kJ/mol;
(5)反应的方程式为2A(g)+B(g)

3C(g),
根据方程式计算,起始时,将C从理论上转化为A、B,
则A的物质的量为2mol+
×0.6mol=2.4mol,B的物质的量为1mol+2 3
×0.6mol=1.2mol,1 3
在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,要达到t1时刻同样的平衡,则所加物质的物质的量必须折算后与原平衡相等.
所以有a+
=2.4,b+2c 3
=1.2,c 3
故答案为:a+
=2.4,b+2c 3
=1.2.c 3

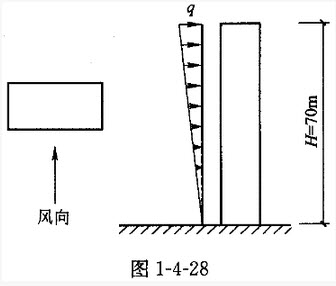
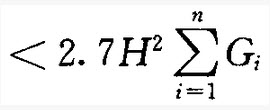 ;又已知,某楼层未考虑重力二阶效应求得的层间位移与层高之比△u/H=1/850。若以增大系数法近似考虑重力二阶效应后,新求得的△u/h比值,则不能满足规范、规程所规定的限值。如果仅考虑用增大EJ值的方法来解决,其他参数不变,试问,结构在该主轴方向的EJ至少需增大到下列何项倍数时,考虑重力二阶效应后该层的△u/h比值,才能满足规范、规程的要求?()
;又已知,某楼层未考虑重力二阶效应求得的层间位移与层高之比△u/H=1/850。若以增大系数法近似考虑重力二阶效应后,新求得的△u/h比值,则不能满足规范、规程所规定的限值。如果仅考虑用增大EJ值的方法来解决,其他参数不变,试问,结构在该主轴方向的EJ至少需增大到下列何项倍数时,考虑重力二阶效应后该层的△u/h比值,才能满足规范、规程的要求?()