Fenton法常用于处理含难降解有机物的工业废水.通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,试探究有关因素对该降解反应速率的影响.
实验中控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表)设计如下对比实验.
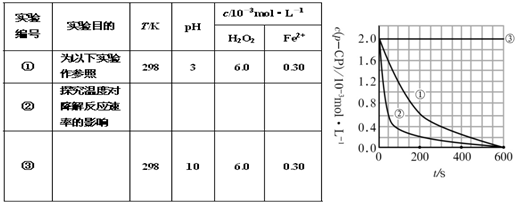
(1)请完成以下实验设计表(表中不要留空格).(数据处理)实验
(2)实验测得p-CP的浓度随时间变化的关系如右上图所示.
a.请根据右上图实验①曲线,计算降解反应在50-300s内的平均反应速率v(p-CP)=______,以及300s时p-CP的降解率.______.
b.实验①②表明温度升高,降解反应速率______.
c.实验③得出的结论是:pH=10时,______.
(3)可通过反应Fe3++SCN-

Fe(SCN)2+来检验反应是否产生铁离子.已知在一定温度下该反应达到平衡时c(Fe3+)=0.04mol•L-1,c(SCN-)=0.1mol•L-1,c[Fe(SCN)2+]=0.68mol•L-1.则此温度下该反应的平衡常数K=______.
解;(1)对比实验的基本思想是控制变量法,温度相同时,变化浓度,在浓度相等时,变化温度,故答案为:313;3;6.0;0.30;探究pH对降解速率的影响;
(2)a.应在50-300s内的平均反应速率v(p-CP)=
=△c t
=4.8×10-6 mol•L-1•s-1,300s时p-CP的降解率=(1.6mol/L-0.4mol/L)×10-3 250s
×100%=80%,故答案为:4.8×10-6mol•L-1•s-1;80%;2mol/L-0.4mol/L 2mol/L
b.根据实验数据内容可以看出温度升高,降解反应速率增大,故答案为:增大;
c.根据实验数据内容可以看出pH=10时,降解速率为零,故答案为:零;
(3)反应Fe3++SCN-

Fe(SCN)2+的平衡常数K=
=[Fe(SCN)2+] [Fe3+][SCN-]
=170{L/mol)0.68 0.04×0.1
故答案为:170.
