问题
多选题
一定条件下在一容积恒为2L的容器内发生反应:2A(g)+B(g)
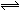
2C(g),已知起始投入4mol A(g) 和2mol B(g),经2s后测得C的浓度为0.6mol/L,并且2s后各组分浓度不再改变.下列说法正确的是( )
A.2s内用物质A表示的平均反应速率为0.3mol/(L•s)
B.2s内用物质B表示的平均反应速率为0.6mol/(L•s)
C.2s后每有0.6mol的物质B生成,同时就有0.6mol物质C生成
D.2s时物质B的浓度为0.7mol/L
答案
A、2s内用物质C表示的平均反应速率为v(C)=
=△c(C) △t
=0.3mol/(L•s),v(A)=v(C)=0.3mol/(L•s),故A正确;0.6mol/L 2s
B、v(B)=
v(C)=1 2
×0.3mol/(L•s)=0.15mol/(L•s),故B错误;1 2
C、0.6mol的物质B生成,表示逆反应方向,同时有0.6mol物质C生成,表示正反应方向,正逆反应速率之比为1:1,不等于系数之比2:1,未处于平衡状态,反应向正反应方向进行,故C错误;
D、△c(B)=)=
△c(C)=1 2
×0.6mol/L=0.3mol/L,2s时物质B的浓度为1 2
-0.3mol/L=0.7mol/L,故D正确.2mol 2L
故选AD
