已知N2O4(无色)

2NO2 (红棕色),在80℃时,将0.80mol的N2O4气体充入4L已经抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
| n( N2O4 )(mol) | 0.80 | a | 0.40 | c | d | e |
| n(NO2)(mol) | 0.00 | 0.48 | b | 1.04 | 1.20 | 1.20 |
(2)反应达到平衡后,将温度升高至100℃,发现颜色加深,则该反应的逆反应是______(填“放热”或“吸热“)
(3)该反应的平衡常数表示式为K=______要增大该反应的K值,可采取的措施有(填序号)______.
(A)向混合气体中通入NO2 (B)使用高效催化剂
(C)升高温度 (D)增大N2O4的起始浓度
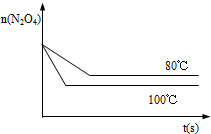
(4)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在100℃时N2O4物质的量的变化曲线(反应物起始的物质的量相等).
(1)根据表中数据可得各时间时反应物和生成物的物质的量,
N2O4(无色)

2NO2
0s时:0.80mol 0
20s时:a 0.48mol
40s时:0.40mol b
80s时:0.20mol 1.20mol
则a=0.80mol-0.24mol=0.56mol;b=0.80mol,
则20s-40s内用NO2表示的平均反应速率为
=0.004mol/(L•S),由表中数据可知,当反应达到80s时反应达到平衡状态,平衡时N2O4的转化率为0.80mol-0.48mol 4L 20s
×100%=75%,0.8mol-0.2mol 0.8mol
故答案为:0.004mol/(L•S);75%;
(2)反应达到平衡后,将温度升高至100℃,发现颜色加深,说明升高温度平衡向正反应方向移动,则正反应为吸热反应,逆反应为放热反应,故答案为:放热;
(3)反应的平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,则为K=
,要增大该反应的K值,应使平衡向正反应方向移动,通入 N2O4和NO2都相当于在原来的基础上缩小体积,则压强增大平衡向逆向移动,K值减小,加入催化剂对平衡没有影响,升高温度平衡右移,K值增大,c2(NO2) c(N2O4)
故答案为:K=
;C;c2(NO2) c(N2O4)
(4)升高温度反应速率增大,平衡右移,平衡时N2O4的物质的量较8℃0时少,故答案为:图象如图所示.