(14分)甲醇被称为21世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇。①CH4(g)+H2O (g) CO(g)+3H2(g) △H1 ②CO(g)+2H2(g)
CO(g)+3H2(g) △H1 ②CO(g)+2H2(g) CH3OH(g)△H2 将0.2mol CH4和0.3mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度.压强的关系如图所示:
CH3OH(g)△H2 将0.2mol CH4和0.3mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度.压强的关系如图所示:
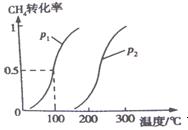
(1)温度不变,缩小体积,增大压强,①的反应速率 (填“增大”.“减小”.“不变”),平衡向 方向移动。
(2)反应①的△H1 0,(填“﹤”“﹦”“﹥”),其平衡常数表达 式为K= ,100℃,压强为p1时平衡常数的值是 。
式为K= ,100℃,压强为p1时平衡常数的值是 。
(3)在压强为0.1Mpa条件下,将a mol CO与3a molH2的混合气体在催化剂作用下进行反应②。为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。请在下空格中填入剩余的实验条件数据。
| 实验编号 | T℃ | n(CO)/n(H2) | p (Mpa) |
| I | 150 | 1/3 | 0.1 |
| Ⅱ | 5 | ||
| Ⅲ | 350 | 5 |
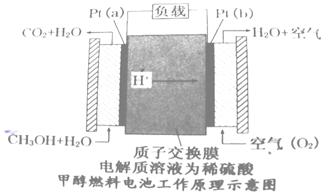
请回答
①Pt(a)电极的电极反应式为
②如果该电池工作时电路中通过2mol电子则消耗的CH3OH有 mol。
(1)增大(1分) 逆反应(或向左)(1分)
(2)﹥(1分) c (CO)·c3(H2)/c (CH4)·c(H2O)(2分) 1.35×10-3(2分)
(3)II 150 1/3 III 1/3 (每空1分共3分)
(4)①CH3OH + H2O -6e- = CO2↑+ 6 H+ (2分)
②1/3 (2分)
