(每空2分,共22分)
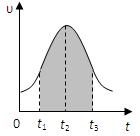
I.实验测得0.01mol/L的KMnO4的硫酸溶液和0.1mol/L的H2C2O4溶液等体积混合后,反应速率υ[mol/(L · s)]与反应时间t(s)的关系如图所示。回答如下问题:
(1)该反应的化学方程式:
(2)0→t2时间段内反应速率增大的原因是: ,
(3)t2→t时间段内反应速率减小的原因是: ,
(4)图中阴影部分“面积”表示t1→t3时间里 。
A.Mn2+物质的量浓度的增大 B.Mn2+物质的量的增加
C.SO42-物质的量浓度 D.MnO4-物质的量浓度的减小
II.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如下图甲、乙所示的实验。请回答相关问题:
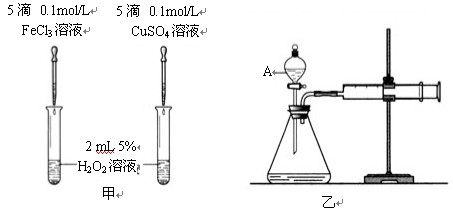
(1)定性分析:如上图甲可观察 ,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是 。
(2)定量分析:如上图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为 ,实验中需要测量的数据是
(3)加入0.01mol MnO2粉末于60mL H2O2溶液中,在标准状况下放出气体体积和时间的关系如图所示。设放出气体的总体积为V mL。
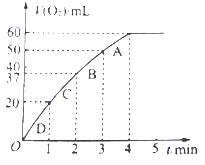
①放出V/3 mL气体时所需时间为 min。
②该H2O2溶液的浓度为
③A、B、C、D各点反应速率快慢的顺序为 > > >
. I.(1)2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 10CO2↑+ 8H2O
(2)反应放热,溶液温度升高,化学反应速率加快
(3)反应物浓度下降,导致反应速率降低
(4)AD
II. 1)产生气泡的快慢 消除阴离子不同对实验的干扰
(2)分液漏斗 产生40mL气体所需的时间
(3)1 ; 0.09mol/L ; D>C>B>A
