问题
选择题
反应3X(g)+Y(g) 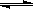 Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.1mol,则此反应的平均速率v为( )
Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.1mol,则此反应的平均速率v为( )
A.V(Y)=0.02mol·L—1·min—1
B.V(Z)=0.10mol·L—1·min—1
C.V(X) =0.03mol·L—1·min—1
D.V(W)=0.02mol·L—1·s—1
答案
答案:C
题目分析:在2L密闭容器中进行,5min内Y减少了0.1mol,所以v(Y)=0.1mol÷2L÷5min=0.01mol/(L•min)。
A、v(Y)=0.1mol÷2L÷5min =0.01mol/(L•min),故A错误;
B、速率之比等于化学计量数之比,所以v(Z)=v(Y)=0.01mol/(L•min),故B错误;
C、速率之比等于化学计量数之比,所以v(X)=3v(Y)=0.03mol/(L•min),故C正确;
D、速率之比等于化学计量数之比,所以v(W)=2v(Y)=0.02mol/(L•min)=1.2mol/(L•S),故D错误.
故选C。
点评:本题考查化学反应速率的计算,难度较小,反应速率计算通常有定义法、化学计量数法,根据情况选择使用。
