问题
选择题
汽车上的催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:
2NO(g)+2CO(g) N2(g)+2CO2(g) DH=-a kJ/mol(a>0)
N2(g)+2CO2(g) DH=-a kJ/mol(a>0)
在某温度时,用气体传感器测得不同时间的NO和CO浓度如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/10-4 mol·L-1 | 10.0 | 4.05 | 2.50 | 1.60 | 1.00 | 1.00 |
| c(CO)/10-3 mol·L-1 | 3.60 | 3.05 | 2.85 | 2.76 | 2.70 | 2.70 |
经分析,得出结论不正确的是
A.2~3 s间的平均反应速率v(NO)=9×10-5 mol/(L·s)
B.催化转化器对废气的转化速率在夏季时比冬季时高
C.若该催化转化器气舱容积为2 L,则达到平衡时反应放出热量1.8a J
D.该温度下,此反应的平衡常数K=5000
答案
答案:C
题目分析:A、化学反应速率v=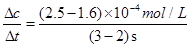 =9×10-5 mol/(L·s),故A正确;B、夏天气温较高气体热胀冷缩使等物质的量的体积增大,使同等状况下的化学平衡向正反应方向进行,使夏天转化率比冬天高,故B正确;C、弱体积增大反应向逆反应方向进行,反应时吸收热量,故C错误;D、2NO(g)+2CO(g)=N2(g)+2CO2(g)
=9×10-5 mol/(L·s),故A正确;B、夏天气温较高气体热胀冷缩使等物质的量的体积增大,使同等状况下的化学平衡向正反应方向进行,使夏天转化率比冬天高,故B正确;C、弱体积增大反应向逆反应方向进行,反应时吸收热量,故C错误;D、2NO(g)+2CO(g)=N2(g)+2CO2(g)
初始浓度:10×10-4 3.6×10-3mol 0 0
变化浓度:9×10-4 9×10-4 9×10-4 9×10-4
平衡浓度:1×10-4 2.7×10-3 9×10-4 9×10-4
即K=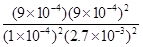 =5000,故D正确。
=5000,故D正确。
