一定温度下,容积为2 L的甲、乙两固定容积的密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g)。达平衡时测得有关数据如下表。
2SO3(g)。达平衡时测得有关数据如下表。
| 容器 | 甲 | 乙 |
| 反应物投入量 | 2 mol SO2、1 mol O2 | 4 mol SO3 |
| n(SO3)/mol | 1.6 | a |
| 反应物的转化率 | α1 | α2 |
下列说法正确的是( )。
A.α1+α2>1
B.1.6<a<3.2
C.若甲中反应2 min时达到平衡,则2 min 内平均速率v(O2)=0.2 mol·L-1·min-1
D.甲平衡后再加入0.2 mol SO2、0.2 mol O2和0.4 mol SO3,平衡正向移动
CD
乙容器中投入4 mol SO3,相当于投入4 mol SO2、2 mol O2,刚好是甲容器投入量的两倍,可以看成是在两个甲容器中分别投入2 mol SO2、1 mol O2,平衡时分别与甲相同。此时,甲中生成的SO3的物质的量正好等于每份容器中剩余的SO3,所以α1+α3=1。然后加压将两份容器压缩成1个甲容器大小,若平衡不移动,各物质的物质的量均不变, n(SO3)= 1.6 mol×2=3.2 mol。由于该反应是气体化学计量数减小的反应,加压平衡正向移动得到更多SO3,所以乙容器中n(SO3)> 3.2 mol,而且α2<α3,即α1+α2<1,A、B错误。
一定温度下,甲容器中:
2SO2(g) + O2(g)  2SO3(g)
2SO3(g)
初始浓度
(mol·L-1) 1 0.5 0
变化浓度
(mol·L-1) 0.8 0.4 0.8
平衡浓度
(mol·L-1) 0.2 0.1 0.8
v(O2)= 0.4 mol·L-1 ÷ 2 min = 0.2 mol·L-1·min-1,C项正确。
平衡常数为:K=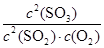 =
=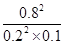 =160。
=160。
D项浓度商为:Qc=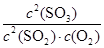 =
=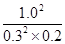 =
=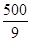 <160,所以平衡正向移动,正确。
<160,所以平衡正向移动,正确。
