问题
选择题
温度为T℃时,向V L的密闭容器中充入一定量的A和B,发生的反应为A(g)+B(g) C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量浓度随时间的变化如表所示。下列说法不正确的是( )
C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量浓度随时间的变化如表所示。下列说法不正确的是( )
| 时间 | 0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min |
| A的物质的量浓度(mol·L-1) | 3.5 | 2.3 | 2.0 | 2.0 | 2.8 | 3.0 | 3.0 |
| B的物质的量浓度(mol·L-1) | 2.5 | 1.3 | 1.0 | 1.0 | 1.8 | 2.0 | 2.0 |
| D的物质的量浓度(mol·L-1) | 0 | 2.4 | 3.0 | 3.0 | 1.4 | 1.0 | 1.0 |
A.前10 min的平均反应速率v(D)=0.3 mol·L-1·min-1
B.该反应的平衡常数表达式为K=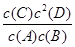
C.若达到平衡时保持温度不变,压缩容器体积,平衡不移动
D.反应至15 min时,改变的条件可以是降低温度
答案
答案:B
A项中,0~10 min,D的物质的量浓度的变化量是3.0 mol·L-1,所以平均反应速度v(D)=3.0 mol·L-1÷10 min=0.3 mol·L-1·min-1,A正确;B项中,因为根据化学反应方程式知C为固体,所以平衡常数表达式中不应含有C物质,B不正确;C项中,根据表格中的数据知15 min时A、B的物质的量浓度均变化了1.5 mol·L-1,D的物质的量浓度变化了3.0 mol·L-1,A、D的物质的量浓度变化量之比为1∶2,所以x=2,该反应在反应前后气体分子数相等,改变容器体积对平衡没有影响,C正确;D项中,根据表格中的数据知15~20 min,A、B的物质的量浓度在增大,D的物质的量浓度在减少,平衡向逆反应方向移动,因为该反应是吸热反应,降低温度时平衡向逆反应方向移动,所以改变的条件可以是降低温度,D正确。
