问题
选择题
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图的所示.下列描述正确的是 ( )
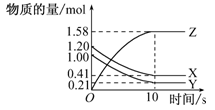
A.从反应开始到10 s末,用Z表示的反应速率为0.158 mol/(L·s)
B.从反应开始到10 s末,用X表示的反应速率为0.79 mol/(L·s)
C.从反应开始到10 s末,Y的转化率为79.0%
D.该反应的化学方程式为X(g)+Y(g)=Z(g)
答案
答案:C
据曲线图可判断出X、Y为反应物、Z为生成物,且该反应为可逆反应.从反应开始到10 s末,Δn(X)=1.20 mol-0.41 mol=0.79 mol, Δn(Y)=1.00 mol -0.21 mol=0.79 mol, Δn(Z)=1.58 mol,所以化学方程式为X+Y 2Z,D错误;0~10 s内,v(Z)=
2Z,D错误;0~10 s内,v(Z)=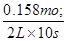 =0.079 mol/(L·s),所以v(X)=
=0.079 mol/(L·s),所以v(X)=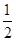 v(Z)=0.0395 mol/(L·s),Y的转化率为
v(Z)=0.0395 mol/(L·s),Y的转化率为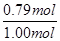 ×100%=79.0%,故A、B错误,C正确。
×100%=79.0%,故A、B错误,C正确。
