已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl-、ClO-、ClO3—三种含氯元素的离子,其中ClO-、ClO3—两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
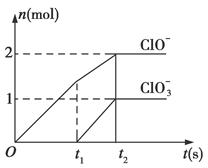
(1)t1前,氧化产物是______________________(填化学式)。
(2)t2时,Ca(OH)2与Cl2发生反应的总的离子方程式:_____________________________。
(3)该石灰乳中含有Ca(OH)2的物质的量是________mol。
(4)NaClO2较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,其爆炸后的产物可能是________(填字母)。
A.NaCl、Cl2
B.NaCl、NaClO
C.NaClO3、NaClO4
D.NaCl、NaClO3(5)配平下列离子方程式:________Fe(OH)3+________ClO-+________OH-=________FeO42—+________Cl-+________H2O。
(1)Ca(ClO)2
(2)5Ca(OH)2+5Cl2=5Ca2++ClO3—+7Cl-+2ClO-+5H2O
(3)5
(4)D
(5)2 (5-n) 2n 2 (5-n) (n+3)
(1)氧化产物即化合价升高后的产物,t1前,从图中直接看出化合价升高的产物只有ClO-,所以氧化产物为Ca(ClO)2;(2)t2时,Ca(OH)2与Cl2反应产物有氯酸钙、次氯酸钙和氯化钙,前两者的物质的量比为1:2,所以总的离子方程式为5Ca(OH)2+5Cl2=5Ca2++ClO3—+7Cl-+2ClO-+5H2O;(3)该石灰乳中含有Ca(OH)2的物质的量可根据上题的方程式进行分析;(4)NaClO2爆炸后的产物可根据化合价有升高有降低进行分析,所以只有D项合理;(5)离子方程式配平基础依据是3个守恒,质量守恒、电荷守恒、化合价升降守恒。
点拨:本题考查氯及其化合物的性质与应用。难度中等。
