二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
(1)工业上制备ClO2的反应原理为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是________。
A.只有还原性
B.还原性和酸性
C.只有氧化性
D.氧化性和酸性②若上述反应中产生0.1 mol ClO2,则转移电子的物质的量为________mol。
(2)目前已开发出用电解法制取ClO2的新工艺。
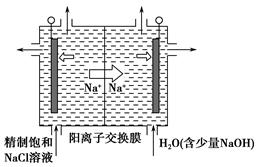
①上图是用石墨作电极,一定条件下电解饱和食盐水制取ClO2的示意图。则阳极产生ClO2的电极反应式为_____________________________________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为________mol,用平衡移动原理解释阴极区pH增大的原因:______________________________________。
(3)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-a mg/L,现用ClO2将CN-氧化,产物中有两种气体生成,其离子反应方程式为________________;处理100 m3这种污水,至少需要ClO2________mol。
(1)①B ②0.1 (2)①Cl--5e-+2H2O=ClO2↑+4H+
②0.01 在阴极上发生反应2H++2e-=H2↑,H+浓度减小,使得H2O
OH-+H+的平衡向右移动,OH-浓度增大,pH增大
(3)2ClO2+2CN-=N2↑+2CO2↑+2Cl- 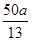
①电解饱和食盐水制取ClO2,ClO2为氧化产物,故应在阳极产生,Cl-失去5个电子生成ClO2,而ClO2中含有氧元素,故还有H2O参加反应,再根据质量守恒配平电极反应式即可。②阴极产生标准状况下112 mL H2,转移电子0.01 mol,消耗的n(H+)=0.01 mol,为保持溶液呈电中性,故有相同物质的量的Na+通过阳离子交换膜移向阴极。阴极上H2O电离出的H+放电,导致H2O的电离平衡向右移动,OH-浓度增大,溶液pH增大。(3)处理污水时生成的两种气体不能具有污染性,应为CO2和N2,再根据得失电子守恒和原子守恒配平即可。由离子反应方程式可知消耗的ClO2的物质的量等于污水中CN-的物质的量,即n(ClO2)=n(CN-)=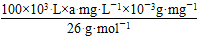 =
=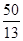 amol。
amol。
