氯气常用于自来水厂杀菌消毒。
(1)工业上用铁电极和石墨做为电极电解饱和食盐水生产氯气,铁电极作 极,石墨电极上的电极反应式为 。
(2)氯氧化法是在碱性条件下,用Cl2将废水中的CN-氧化成无毒的N2和CO2。该反应的离子方程式为 。
(3)氯胺(NH2Cl)消毒法是在用液氯处理自来水的同时通入少量氨气,发生反应:Cl2 + NH3 = NH2Cl + HCl,生成的NH2Cl比HClO稳定,且能部分水解重新生成HClO,起到消毒杀菌的作用。
①氯胺能消毒杀菌的原因是 (用化学用语表示)。
②氯胺消毒法处理后的水中,氮元素多以NH4+的形式存在。
已知:NH4+(aq) + 1.5O2(g)= NO2-(aq) + 2H+(aq) + H2O (l) ΔH=-273 kJ·mol-1
NH4+(aq) + 2O2(g)= NO3-(aq) + 2H+(aq) + H2O (l) ΔH =-346 kJ·mol-1
NO2-(aq)被O2氧化成NO3-(aq)的热化学方程式为 。
(4)在水产养殖中,可以用Na2S2O3将水中残余的微量Cl2除去,某实验小组利用下图所示装置和药品制备Na2S2O3。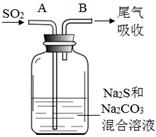
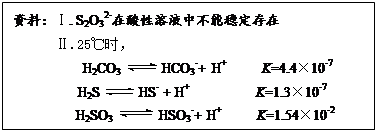
结合上述资料回答:
开始通SO2时,在B口检测到有新的气体生成,判断从B口排出的气体中是否含有H2S,并写出判断依据 。
为获得较多的Na2S2O3,当溶液的pH接近7时,应立即停止通入SO2,其原因是 。
(1)阴 2Cl- - 2e- = Cl2↑
(2)5Cl2 + 2CN- + 4H2O = 10Cl- + N2↑+ 2CO2↑+ 8H +
(3)① NH2Cl+ H2O  NH3 + HClO(不写可逆号扣1分)
NH3 + HClO(不写可逆号扣1分)
② 2NO2- (aq) + O2(g) = 2NO3-(aq) ΔH = -146 kJ·mol-1(反应热写错扣1分)
(4)①答案1:含H2S,由电离常数知H2SO3酸性强于H2S,溶液中的S2-与H2SO3反应生成H2S。
答案2:不含H2S,S2-还原性较强,能被SO2氧化生成其它含硫物质。
(只写“含”或“不含”为0分)
②通入过多SO2会使溶液的pH小于7,S2O32-在酸性溶液中不能稳定存在。
题目分析:(1)工业上用铁电极和石墨做为电极电解饱和食盐水生产氯气,铁电极不能做阳极,如果做阳极,Fe-2e-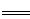 Fe2+,不会得到氯气,所以铁电极作阴极,石墨电极上的电极反应式为2Cl- - 2e- = Cl2↑。
Fe2+,不会得到氯气,所以铁电极作阴极,石墨电极上的电极反应式为2Cl- - 2e- = Cl2↑。
(2)氯氧化法是在碱性条件下,用Cl2将废水中的CN-氧化成无毒的N2和CO2。
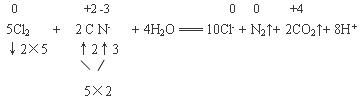
(3)①氯胺能消毒杀菌的原因是发生了水解NH2Cl+ H2O  NH3 + HClO,HClO具有强氧化性,能消毒杀菌。
NH3 + HClO,HClO具有强氧化性,能消毒杀菌。
②NH4+(aq) + 1.5O2(g)= NO2-(aq) + 2H+(aq) + H2O (l) ΔH=-273 kJ·mol-1 ①
NH4+(aq) + 2O2(g)= NO3-(aq) + 2H+(aq) + H2O (l) ΔH =-346 kJ·mol-1 ②
②×2-①×2得NO2-(aq)被O2氧化成NO3-(aq)的热化学方程式为 2NO2- (aq) + O2(g) = 2NO3-(aq) ΔH = -146 kJ·mol-1;
(4)①开始通SO2时,在B口检测到有新的气体生成,判断从B口排出的气体中是否含有H2S,答案1:含H2S,由电离常数知H2SO3酸性强于H2S,溶液中的S2-与H2SO3反应生成H2S。
答案2:不含H2S,S2-还原性较强,能被SO2氧化生成其它含硫物质。
②为获得较多的Na2S2O3,当溶液的pH接近7时,应立即停止通入SO2,其原因是通入过多SO2会使溶液的pH小于7,S2O32-在酸性溶液中不能稳定存在。
