(19分)碳及其化合物有广泛的用途。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
C(s)+ H2O(g)  CO(g) +H2(g) ΔH=" +131.3" kJ•mol-1,以上反应达到平衡后,在体积不变的条件下,以下措施加快反应速率且有利于提高H2O的平衡转化率的是 。(填序号)
CO(g) +H2(g) ΔH=" +131.3" kJ•mol-1,以上反应达到平衡后,在体积不变的条件下,以下措施加快反应速率且有利于提高H2O的平衡转化率的是 。(填序号)
A.升高温度
B.增加碳的用量
C.加入催化剂
D.用CO吸收剂除去CO E.增大压强(2)又知,C(s)+ CO2(g) 2CO(g) △H=+172.5kJ•mol-1
2CO(g) △H=+172.5kJ•mol-1
写出C(s)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式 。
(3)甲醇是一种燃料,可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,该电池负极反应式为: 。
若用该电池提供的电能电解600mLNaCl溶液,设有0.01molCH3OH完全放电,NaCl足量,且电解产生的Cl2全部溢出,电解前后忽略溶液体积的变化,则电解结束后所得溶液的pH=
(4)将一定量的CO(g)和H2O(g)分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:
CO(g)+H2O(g)  CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
| 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所x需时间/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
改变反应的某一条件,反应进行到tmin时,测得混合气体中CO2的物质的量为0.6 mol。若用200 mL 4.5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示) 。
(5)工业生产是把水煤气中的混合气体经过处理后获得的较纯H2用于合成氨。合成氨反应原理为:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJ•mol-1。实验室模拟化工生产,分别在不同实验条件下反应,N2浓度随时间变化如下图。
2NH3(g) ΔH=-92.4kJ•mol-1。实验室模拟化工生产,分别在不同实验条件下反应,N2浓度随时间变化如下图。
不同实验条件下反应,N2浓度随时间变化如下图1。
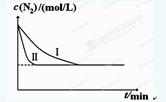

图1 图2
请回答下列问题:
①与实验Ⅰ比较,实验Ⅱ改变的条件为 。
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在上图2中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图。
(1)A (2分)
(2)C(s)+2H2O(g)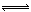 CO2(g)+2H2(g) ∆H="90.1" kJ•mol-1(3分)
CO2(g)+2H2(g) ∆H="90.1" kJ•mol-1(3分)
(3)CH3OH(g) +8OH‾-6e-=CO32‾ +6H2O (3分) 13(2分)
(4)K=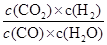 =
=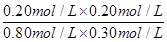 =0.17 (3分)
=0.17 (3分)
2CO2 +3OH- ===CO32- + HCO3- + H2O (3分)
(5)①使用催化剂(1分)。
②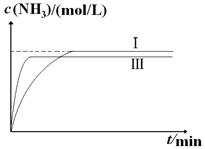 (2分,纵坐标起点可以大于0。Ⅲ比Ⅰ快1分,比Ⅰ少1分)
(2分,纵坐标起点可以大于0。Ⅲ比Ⅰ快1分,比Ⅰ少1分)
题目分析:(1)A、升高温度,化学反应速率加快,正反应为吸热反应,平衡向正反应方向移动,提高H2O的平衡转化率,正确;B、碳为固体,增加碳的量,反应速率和平衡都不变,错误;C、加入催化剂,平衡不移动,错误;D、用CO吸收剂除去CO可提高H2O的平衡转化率,但反应速率减小,错误;E、增大压强,平衡向逆反应方向移动,H2O的平衡转化率减小,错误。
(2)首先写出C(s)与H2O(g)反应生成CO2(g)和H2(g)的化学方程式并注明状态,C(s)+2H2O(g)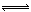 CO2(g)+2H2(g),然后根据盖斯定律求焓变,∆H=2∆H1—∆H2="2×131.3" kJ•mol-1—172.5kJ•mol-1="90.1" kJ•mol-1,可得热化学方程式。
CO2(g)+2H2(g),然后根据盖斯定律求焓变,∆H=2∆H1—∆H2="2×131.3" kJ•mol-1—172.5kJ•mol-1="90.1" kJ•mol-1,可得热化学方程式。
(3)甲醇在电池负极上失去电子,KOH溶液作电解质溶液,生成CO32‾和H2O,配平可得电解方程式:CH3OH(g) +8OH‾-6e-=CO32‾ +6H2O;电池和电解池通过的电量相等,根据电极方程式和电子转移可得:CH3OH ~ 6e‾ ~ 6OH‾,则n(OH‾)=6n(CH3OH)=0.06mol,则c(OH‾)=0.06mol÷0.6L=0.1mol•L‾1,可得pH=13。
(4)根据三段式进行计算:
H2O (g) + CO(g) 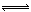 H2(g) + CO2(g)
H2(g) + CO2(g)
起始浓度(mol•L‾1) 0.5 1 0 0
转化浓度(mol•L‾1) 0.2 0.2 0.2 0.2
平衡浓度(mol•L‾1) 0.3 0.8 0.2 0.2
K=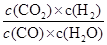 =
=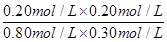 =0.17
=0.17
若CO2与NaOH的物质的量之比为1:1,生成NaHCO3,若CO2与NaOH的物质的量之比为1:2,生成Na2CO3,题目所给CO2物质的量为0.6mol,NaOH的物质的量为:0.2L×4.5mol•L‾1=0.9mol,二者物质的量之比为2:3,生成CO32‾和HCO3‾,配平可得离子方程式:2CO2 +3OH- ===CO32- + HCO3- + H2O
(5)根据图像可知实验Ⅱ反应速率加快,但化学平衡没有移动,所以实验Ⅱ改变的条件为使用了催化剂;实验Ⅲ比实验Ⅰ的温度要高,反应速率加快,因为该反应为放热反应,所以升温平衡向逆反应方向移动,平衡时NH3的平衡浓度减小,可画出图像。
