问题
选择题
下列热化学方程式或离子方程式中,正确的是
A.0.01mol·L-1NH4Al(SO4)2溶液与0.02mol·L-1Ba(OH)2溶液等体积混合:
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B.一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
N2(g)+3H2(g) 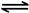 2NH3(g)△H=-38.6kJ·mol-1
2NH3(g)△H=-38.6kJ·mol-1
C.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓
D.CO(g)的燃烧热是283.0 kJ·mol-1,则CO2分解的热化学方程式为: 2CO2(g) =2CO(g)+O2(g) ΔH=+283.0 kJ·mol-1
答案
答案:A
题目分析:A、NH4Al(SO4)2与Ba(OH)2物质的量之比为1:2,生成BaSO4、Al(OH)3和NH3•H2O,正确;B、因为N2和H2的反应为可逆反应,0.5mol N2(g)和1.5molH2(g)只能部分反应,无法计算焓变,错误;C、溴乙烷中含有Br原子,不是Br‾,与AgNO3溶液不反应,错误;D、燃烧热是指1mol可燃物充分燃烧,生成稳定的氧化物所放出的能量,所以CO2分解的热化学方程式为:2CO2(g) =2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1,错误。
